Truyền thông sức khỏe
Nhiễm khuẩn gram dương kháng thuốc
NHIỄM KHUẨN GRAM DƯƠNG KHÁNG THUỐC
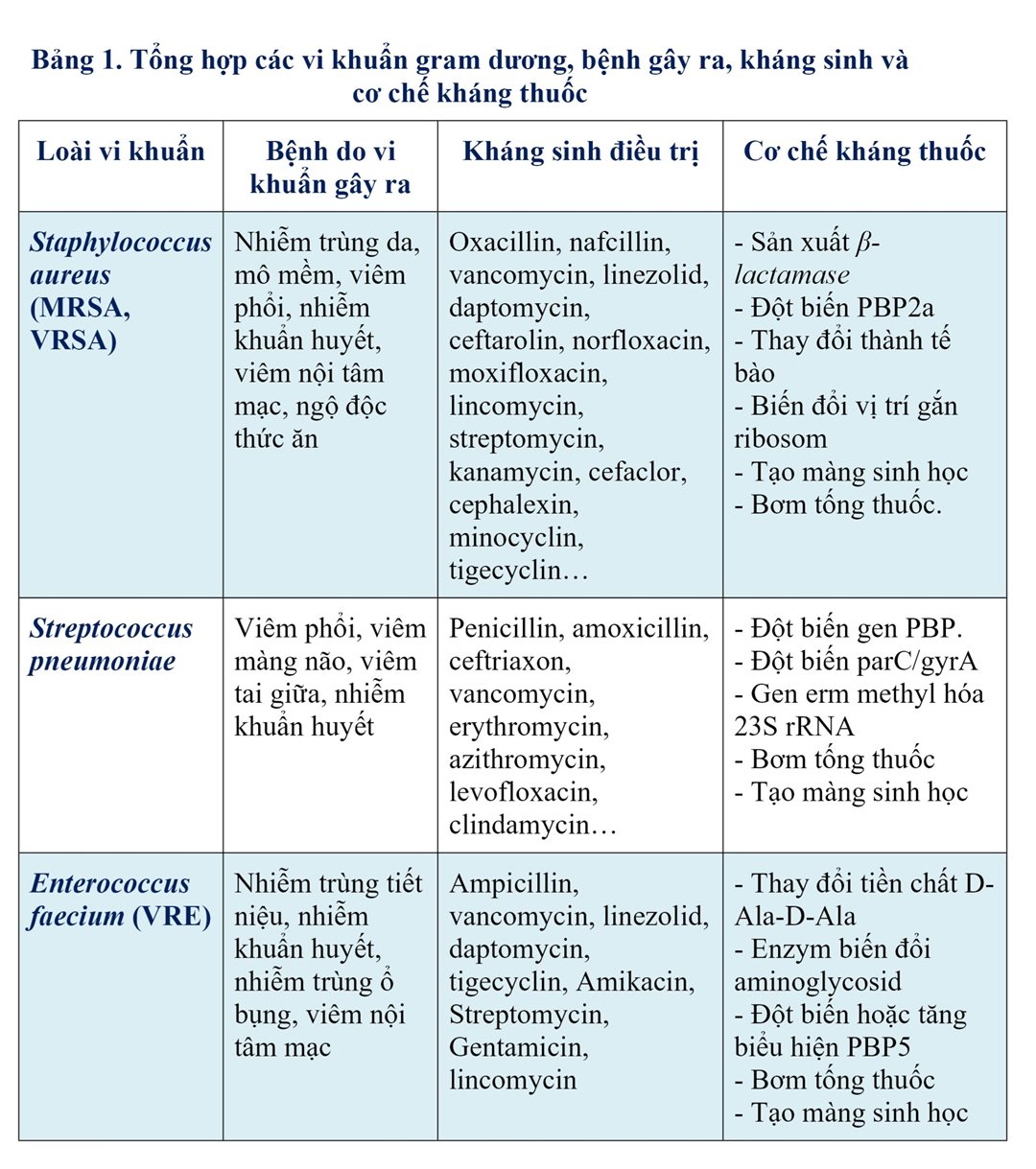
Tình trạng kháng kháng sinh của vi khuẩn Gram dương đang gia tăng nhanh chóng, trở thành vấn đề toàn cầu nghiêm trọng ảnh hưởng đến hệ thống y tế và kinh tế. Bao gồm: Staphylococcus aureus, Streptococcus pneumoniae và Enterococcus faecium. Các cơ chế kháng thuốc chủ yếu ở vi khuẩn Gram dương như bất hoạt enzyme, biến đổi đích tác dụng, giảm hấp thu thuốc và tăng cường bơm đẩy thuốc.
- 1. Giới thiệu
Kháng kháng sinh (KKS) là mối đe dọa nghiêm trọng đối với sức khỏe toàn cầu, xảy ra khi vi khuẩn thích nghi để chống lại tác dụng của các kháng sinh. Khi đó, các phương pháp điều trị thông thường mất hiệu quả, làm tăng tỷ lệ mắc bệnh, tử vong và gánh nặng kinh tế.
Sự lạm dụng và sử dụng sai kháng sinh trong y tế, thú y và nông nghiệp là nguyên nhân chính gây KKS:
- - Dùng thuốc khi không cần thiết về mặt lâm sàng;
- - Thuốc kém chất lượng;
- - Tự ý dùng thuốc hoặc kê đơn sai cho bệnh do virus;
- - Lạm dụng kháng sinh trong bệnh viện;
- - Dùng kháng sinh trong chăn nuôi, dẫn đến truyền vi khuẩn kháng thuốc từ động vật sang người;
- - Thải kháng sinh ra môi trường, khiến vi khuẩn tiến hóa và đột biến kháng thuốc.
Theo thống kê:
- Mỗi năm có 7,7 triệu ca tử vong do nhiễm khuẩn, trong đó 4,95 triệu liên quan đến vi khuẩn kháng thuốc và 1,27 triệu tử vong trực tiếp do kháng kháng sinh.
- Tại Châu Âu, thiệt hại kinh tế do KKS ít nhất 1,5 tỷ euro/năm. Tại Hoa Kỳ, tổng chi phí lên đến 55 tỷ USD/năm.
WHO (2024) công bố danh sách ưu tiên toàn cầu các mầm bệnh kháng thuốc, chia thành ba nhóm: nghiêm trọng – cao – trung bình, nhằm định hướng nghiên cứu phát triển thuốc mới.
Trong đó, các vi khuẩn Gram dương đáng chú ý gồm:
- - Methicillin-resistant Staphylococcus aureus (MRSA) – kháng nhiều loại kháng sinh.
- - Vancomycin-resistant Enterococcus faecium (VRE) – kháng vancomycin và nhiều thuốc khác.
- - Streptococcus pneumoniae – thuộc nhóm ưu tiên trung bình.
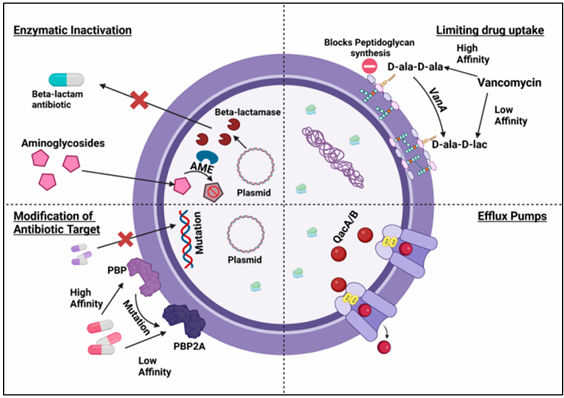
Cơ chế KKS của vi khuẩn Gram dương
- - Bất hoạt enzyme.
- - Biến đổi đích tác dụng của thuốc.
- - Giảm hấp thu thuốc.
- - Tăng thải thuốc ra ngoài.
Hình 1. Cơ chế đề kháng kháng sinh của vi khuẩn Gram dương
- 2. Một số vi khuẩn Gram dương kháng thuốc
2.1 Staphylococcus aureus
Staphylococcus aureus (S. aureus) là vi khuẩn Gram dương thuộc họ Micrococcaceae, thường cư trú ở da và mũi người. Nó gây nhiều loại nhiễm trùng (da, mô mềm, cơ quan nội tạng), có thể nặng và đe doạ tính mạng. S. aureus tạo nhiều protein bám bề mặt và tiết ra ngoại bào, giúp gây bệnh trong cộng đồng và bệnh viện (vết mổ, thiết bị y tế). Ngộ độc thức ăn có thể xảy ra khi ăn thực phẩm nhiễm độc tố của vi khuẩn. Hai thập kỷ qua, tỉ lệ nhiễm S. aureus tăng rõ trong cộng đồng và bệnh viện; MRSA nằm trong danh sách ưu tiên cao của WHO từ 2017. Tại châu Á, MRSA lưu hành rộng, nhiều nơi có tỉ lệ rất cao.
Điều trị MSSA thường dùng oxacillin, nafcillin, cefazolin, cephalothin; tuy nhiên S. aureus hay kháng methicillin. Với MRSA, vancomycin là thuốc điều trị chính.
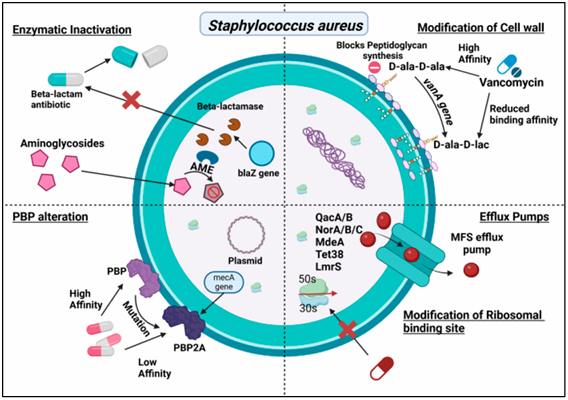
Cơ chế kháng thuốc chính của S. aureus:
- - β-lactamase: thuỷ phân vòng β-lactam. Kháng cao với cloxacillin, ceftriaxon, amoxicillin; ngay cả amoxicillin + clavulanat có thể kém hiệu quả khi vi khuẩn sản xuất β-lactamase mạnh.
- - Biến đổi aminoglycosid: các enzyme APH/AAC/ANT (gen phổ biến: aac(6')-Ie-aph(2''), aph(3')-IIIa, ant(4')-Ia) bất hoạt nhóm thuốc; liên quan kháng gentamicin, tobramycin, kanamycin…
- - Biến đổi thành tế bào và đích vancomycin:
- VanA/Tn1546 đổi D-Ala-D-Ala → D-Ala-D-Lac, giảm ái lực vancomycin.
- Dày thành tế bào giữ “bẫy” vancomycin, giảm ức chế tổng hợp peptidoglycan.
- Thay đổi điện tích bề mặt qua MprF (gắn L-lysin/L-alanin lên phosphatidylglycerol) làm giảm nhạy với peptid kation và vancomycin, gentamicin, daptomycin.
- - Tạo màng sinh học (biofilm): tỷ lệ hình thành biofilm cao; phần lớn chủng tạo biofilm là đa kháng và nhiều chủng là MRSA.
- - Thay đổi PBP (mecA/PBP2a): nhận mecA (PBP2a ái lực β-lactam thấp) → kháng methicillin, penicillin mở rộng, cephalosporin; làm tăng MIC nhiều β-lactam.
- - Biến đổi vị trí gắn trên ribosom:
- Tet(M)/Tet(S) giải phóng tetracyclin khỏi 30S → kháng tetracyclin (đặc biệt minocyclin do Tet(M)).
- Đột biến rplV (L22), rplD (L4) → kháng macrolid, streptoGramin;
- Thay đổi L3/L4 và đột biến rrl5 (23S rRNA, T2500A) → kháng linezolid.
- - Bơm tống thuốc: >30 bơm tiềm năng.
- MFS: Tet(K/L/38/42/43/45/63) (tetracyclin), NorA/NorB/NorC (fluoroquinolon), SdrM, MdeA, LmrS (đa thuốc). Điều hoà bởi MgrA.
- SMR: QacA/B (kháng chất sát khuẩn QACs, chlorhexidin; điều hoà QacR), QacC/Ebr, QacD/Smr, SepA.
- MATE: MepA (điều hoà bởi cụm mepRAB).
- ABC: SAV1866 (mô hình cấu trúc), AbcA (liên quan β-lactam kỵ nước, tự phân thành tế bào; điều hoà MgrA).
Hình 2. Cơ chế đề kháng kháng sinh của S. aureus
2.2 Streptococcus pneumoniae
Streptococcus pneumoniae (S. pneumoniae) là vi khuẩn Gram dương thuộc họ Streptococcaceae, gây viêm phổi, viêm màng não, viêm tai giữa… Vi khuẩn cư trú ở niêm mạc hô hấp và lây qua giọt bắn; dễ bùng phát dịch. Trẻ em, người già, người suy giảm miễn dịch là nhóm dễ tổn thương. Phế cầu đã thích nghi với nhiều nhóm kháng sinh và dần biểu hiện kháng thuốc.
Điều trị: chủng nhạy cảm dùng penicillin; nhưng kháng β-lactam cùng kháng macrolid, fluoroquinolon, cotrimoxazol ngày càng phức tạp. Viêm màng não do phế cầu thường phối hợp vancomycin.
Vaccin: có PPV (polysaccharid) và PCV (liên hợp). Sau khi triển khai tiêm vaccin PCV7 tại Hoa Kỳ, số ca mắc do chủng kháng penicillin, đa kháng giảm đáng kể (1999→2004: từ 6,3 còn 2,7/100.000). Dù vậy, nhiễm trùng hô hấp do S. pneumoniae vẫn là gánh nặng toàn cầu; WHO ước ~1,6 triệu ca tử vong/năm.
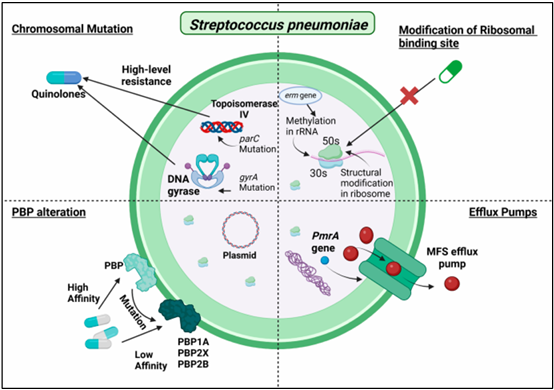
Cơ chế kháng thuốc chính của S. pneumoniae:
Không tạo β-lactamase; enzyme sửa đổi aminoglycosid hiếm gặp hơn so với S. aureus, Enterococcus.
- - Biến đổi PBP: S. pneumoniae biến nạp tự nhiên, hình thành PBP “khảm” (PBP1A, 1B, 2A, 2B, 2X). Đột biến, trao đổi gen làm giảm ái lực với β-lactam, đặc biệt PBP1A/2X/2B liên quan mức kháng penicillin cao; ví dụ đột biến PBP2X (Gln552→Glu).
- - Đột biến nhiễm sắc thể – fluoroquinolon: diễn tiến 2 bước: trước parC (Topo IV) → kháng mức thấp, sau gyrA (DNA gyrase) → kháng mức cao.
- - Sửa đổi vị trí gắn ribosom:
- Macrolid–lincosamid–streptoGramin: gen erm methyl hoá 23S rRNA → giảm gắn thuốc → kháng erythromycin, azithromycin, clarithromycin, clindamycin.
- Tetracyclin: tet(M)/tet(O) bảo vệ ribosom 30S, cản tetracyclin gắn A/P-site.
- - Bơm tống thuốc:
- PmrA/MFS góp phần giảm nhạy fluoroquinolon.
- MefE bơm tống macrolid.
- Biofilm: nhiều gen tham gia hình thành, giải tán; biofilm tạo môi trường thuận lợi cho chuyển gen ngang (HGT) và duy trì kiểu hình kháng.
Hình 3. Cơ chế đề kháng kháng sinh của S. pneumoniae
2.3 Enterococcus faecium
Enterococcus faecium (E. faecium) là vi khuẩn Gram dương hình cầu, sống trong đường ruột người, đã trở thành tác nhân gây nhiễm khuẩn bệnh viện nghiêm trọng. Nó gây nhiễm trùng tiết niệu, nhiễm trùng ổ bụng, viêm nội tâm mạc và nhiễm khuẩn huyết.
Ở châu Âu, Enterococcus đứng thứ 2 về nhiễm trùng vết thương và tiết niệu; thứ 3 về nhiễm khuẩn huyết. Ở Hoa Kỳ, khoảng 12% nhiễm khuẩn bệnh viện có liên quan đến Enterococcus spp.
Vi khuẩn có khả năng kháng thuốc cao, nhờ nhiều plasmid và transposon chứa gen kháng erythromycin, gentamicin, kanamycin, streptomycin, tetracyclin và vancomycin. Đa số chủng E. faecium kháng vancomycin (VRE), trong đó VanA và VanB là phổ biến nhất. Enterococcus còn là nguồn dự trữ gen kháng thuốc, có thể truyền gen này sang các vi khuẩn Gram dương khác (như S. aureus), gây lan rộng tình trạng kháng kháng sinh trong bệnh viện.
Vi khuẩn được phát hiện trong pho mát, sữa lên men, thịt bò, thịt heo, gia cầm… → có thể truyền vi khuẩn kháng thuốc sang người qua thực phẩm.
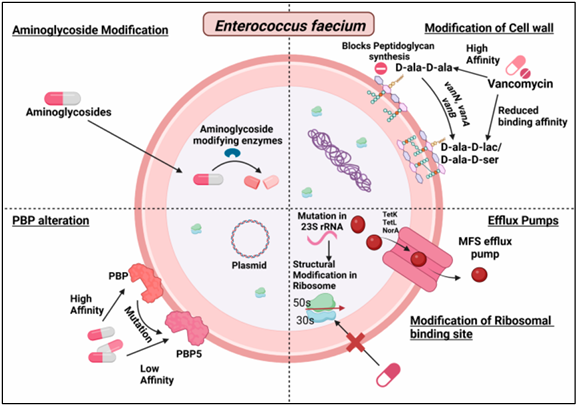
Cơ chế kháng thuốc của E. faecium
- - Biến đổi aminoglycosid:
- Gen aph(2'')-Ic, aph(2'')-Id, aph(2'')-Ib → kháng amikacin.
- Kháng streptomycin (50–60%), gentamicin (20–80%).
- Enzyme AAC(6′)-Ii và EfmM gây kháng tự nhiên tobramycin, kanamycin.
- Đột biến protein ribosom S12 hoặc gen ANT(3'')-Ia, ANT(6')-Ia → kháng streptomycin mức cao.
- - Biến đổi thành tế bào: Thay D-Ala-D-Ala → D-Ala-D-Lac hoặc D-Ala-D-Ser, làm giảm ái lực của vancomycin.
- VanA: kháng cao cả vancomycin & teicoplanin (MIC > 64 mg/L).
- VanB: kháng vancomycin ở nhiều mức, vẫn nhạy teicoplanin.
- VanN: tạo tiền chất D-Ala-D-Ser → kháng trung bình (MIC 8–16 mg/L).
- Tạo biofilm: Gen esp là yếu tố chính giúp bám dính và tồn tại trong môi trường bệnh viện. Chủng VRE tạo màng mạnh, kháng nhiều thuốc (ampicillin, vancomycin, linezolid, gentamicin).
- - Biến đổi vị trí gắn ribosom:
- Đột biến G2576T trong 23S rRNA → kháng linezolid.
- Gen cfr mã hóa enzyme methyltransferase → methyl hóa A2503 (23S rRNA) → kháng linezolid, phenicol, lincosamid, pleuromutilin.
- Đột biến gyrA, parC → kháng fluoroquinolon.
- Thay đổi PBP: tăng biểu hiện hoặc đột biến PBP5 → giảm ái lực với β-lactam, đặc biệt ampicillin.
- Bơm tống thuốc:
- Gồm MsrC, Tet(K), Tet(L) (thuộc nhóm MFS), dùng năng lượng proton để tống tetracyclin (trừ tigecyclin).
- Có thể có bơm tương tự NorA → kháng fluoroquinolon.
Hình 4. Cơ chế đề kháng kháng sinh của E. faecium
- 3. Kháng sinh điều trị vi khuẩn Gram dương kháng thuốc
Trong thập kỷ qua, một số kháng sinh mới đã ra đời giúp giải quyết tình trạng kháng thuốc. Các cephalosporin mới gồm ceftobiprol, ceftarolin, cefiderocol, ceftolozan + tazobactam.
- Ceftobiprol (thế hệ 5) là β-lactam đầu tiên có hiệu quả trên MRSA và VRSA nhờ gắn tốt vào PBP2a, PBP2x (quan trọng cả ở S. pneumoniae).
- Delafloxacin (2017) là fluoroquinolon phổ rộng, tác dụng trên MRSA và P. aeruginosa, có đường uống và tiêm để điều trị nhiễm trùng da cấp tính do vi khuẩn đề kháng.
- Lefamulin (2019 FDA, 2020 EC), thuộc pleuromutilin, điều trị viêm phổi cộng đồng do S. pneumoniae, S. aureus; ức chế tổng hợp protein bằng cách gắn trung tâm peptidyl-transferase của 50S.
Các loại kháng sinh mới được phát triển với mục tiêu vượt qua những cơ chế kháng thuốc hiện có, nhưng chúng thường chỉ được dùng như “lựa chọn cuối cùng” để tránh vi khuẩn nhanh chóng kháng trở lại. Mặc dù đã có một số tiến bộ, số lượng thuốc mới thật sự hiệu quả với các vi khuẩn nguy hiểm vẫn còn rất ít, khiến việc đánh giá hiệu quả thực tế trở nên khó khăn và cho thấy sự cần thiết phải đẩy mạnh nghiên cứu – phát triển kháng sinh mới.
TÀI LIỆU THAM KHẢO
Rajput P, Nahar KS, Rahman KM. Evaluation of Antibiotic Resistance Mechanisms in Gram-Positive Bacteria. Antibiotics (Basel). 2024 Dec 8;13(12):1197. doi: 10.3390/antibiotics13121197. PMID: 39766587; PMCID: PMC11672434.
Ths. Kim Ngọc Sơn
Ths. Đinh Thị Thúy Hà